Modern chemistry lesson: examples of opportunities for conducting laboratory classes
Modern chemistry lesson: examples of opportunities for conducting laboratory classes
Abstract
The article examines contemporary approaches to conducting chemistry laboratory classes in the school education system, analyses the role of practical activities in the development of key competencies in students, and emphasises the necessity of integrating traditional methods with modern digital technologies, such as virtual laboratories, simulators, and augmented reality tools.
Examples of practical laboratory classes are presented, including the use of a digital microscope, pH meter, conductometer and thermocouple, and the stages of performing the work and recording the results are described.
Particular attention is paid to the prospects for the development of laboratory classes, taking into account digitalisation and project-based teaching methods, which contribute to the development of research skills, critical thinking and motivation among schoolchildren. The importance of creating a flexible, interactive teaching system capable of preparing students for modern challenges and professional activities is emphasised.
1. Введение
В условиях постоянного и быстрого развития современных технологий крайне важно не только передавать теоретические знания во время уроков, но и необходимо формировать у школьников практические умения, научить своих учеников видеть смысл в окружающих явлениях, применять свои умения на практике, а также развить их критическое мышление. В этом контексте лабораторные занятия в системе образования имеют важное значение: они позволяют не только запомнить теоретический материал, но и понять механизмы природных явлений и научиться использовать их для решения практических задач, ощутить себя участниками научного процесса
.Несмотря на важность практической деятельности в обучении химии, современные требования к качеству образования, а также внедрение новых педагогических технологий и методов, требуют переосмысления традиционных подходов к организации лабораторных работ
. В условиях цифровизации, качественных и количественных изменений в системе образования возникают актуальные вопросы: как повысить эффективность лабораторных занятий по химии, сделать их более интересными и запоминающимися? Какие методы и средства способны помочь педагогам раскрыть потенциал современного школьника, обеспечить развитие необходимых практических навыков, которые нужны для успешной адаптации к жизни (критического мышления, креативности, умения работать в команде и других)?Цель исследования — проанализировать современные подходы к организации лабораторных занятий по химии, определить их роль в формировании научных знаний и практических навыков современных школьников, выявить возможности модернизации лабораторных работ с учетом современных технологий и цифровых средств.
Задачи исследования включают:
1. Анализ роли проведения лабораторных работ по химии в школе.
2. Разработка рекомендаций по внедрению подходов в учебный процесс для повышения мотивации и качества обучения школьников, примеры лабораторных работ с использованием современного школьного оборудования.
3. Анализ перспектив и путей развития лабораторных работ в современном мире.
2. Роль лабораторных занятий в современном обучении химии
Лабораторные занятия по химии являются неотъемлемой частью современной системы обучения естественнонаучным предметам, они играют важную роль в формировании профессиональных и общих компетенций школьников , . Их важное значение обусловлено тем, что практическая деятельность в рамках лабораторных работ создает условия для активного освоения теоретического материала, а также способствует развитию исследовательских навыков и умения применять приобретённые знания в конкретных ситуациях.
Практическая деятельность в лабораторных условиях позволяет школьникам не только закрепить изученные химические закономерности на практике, но и сформировать представление о свойствах окружающих веществ, механизмах протекания химических реакций и экспериментальных методах исследования веществ. Здесь лабораторные занятия выступают как средство перехода от абстрактных теоретических понятий к их практическому воплощению, что способствует повышению уровня усвоения учебного материала и развитию начального научного мировоззрения
.Кроме того, лабораторные работы способствуют развитию таких личностных качеств, как аккуратность, ответственность, внимательность и терпение
. Эти качества являются важными составляющими формирования профессиональной этики у школьников — в процессе проведения экспериментов учащиеся учатся соблюдать технику безопасности, правильно работать с химическими веществами и обращаться с приборами.Современные педагогические подходы предполагают тесную связь традиционных методов с цифровыми технологиями, что расширяет возможности лабораторных занятий
, , . Использование виртуальных лабораторий, мультимедийных средств обучения, а также ряда химических симуляторов позволяет моделировать химические процессы, наблюдать реакции в интерактивной форме, что повышает мотивацию и интерес школьников к изучению химии. Такой подход способствует более глубокому пониманию и закреплению теоретического материала, а также развивает навыки самостоятельного поиска информации и анализа.В целом, внедрение современных технологий и методов проведения экспериментов способствует повышению эффективности обучения, делает его более интересным и доступным, а лабораторные занятия выступают важнейшим инструментом формирования у школьников научной культуры, расширяя познавательные горизонты.
3. Примеры возможностей для проведения лабораторных занятий в рамках школьной программы
В качестве примера приведём лабораторную работу, которая может быть использована в рамках практикума в профильных классах естественно-научной, медицинской, химической профилизации. Для простоты восприятия приведём также и стандартную форму лабораторной работы, которая состоит из следующих элементов:
1) название лабораторной работы;
2) цель;
3) материалы для исследования;
4) реактивы, посуда, оборудование;
5) ход работы;
6) оформление результатов (в виде таблицы, если это возможно);
7) вывод.
Такая комплексная работа может быть разделена на отдельные части, которые можно использовать как самостоятельные лабораторные или практические работы. Рассмотрим пример работы под названием «Физико-химический анализ солей и их растворов: диссоциация и гидролиз».
1. Микроскопия кристаллов солей с использованием цифрового микроскопа
Кристаллы — это твердое состояние веществ, характеризующееся регулярной и упорядоченной решетчатой структурой. Морфология кристаллов зависит от свойств вещества, условий кристаллизации, скорости охлаждения и концентрации раствора. Микроскопия – это метод исследования объектов с помощью микроскопа, позволяющий рассматривать структуры, невидимые невооруженным глазом. Современные цифровые микроскопы объединяют оптическое увеличение с возможностью подключения к компьютеру, что обеспечивает высокое качество изображений, их фиксацию и последующий анализ.
Цель: научиться пользоваться цифровым микроскопом, изучить строение кристаллов солей.
Материалы для исследования: кристаллы солей NaCl, CuSO4 ×5H2O, Na2CO3.
Реактивы, посуда, оборудование: цифровой USB-микроскоп ProScope HR (модель BD-DLX, производство Vernier, США на рис. 1), лопатки для отбора проб, лодочки, электронные весы, исследуемые соли.

Рисунок 1 - Цифровой USB-микроскоп ProScope HR (BD-DLX, Vernier, США)
1. С помощью учителя собрать лабораторную установку, как показано на рис. 2, подключить камеру к компьютеру, настроить разрешение, при необходимости включить светодиодную подсветку.

Рисунок 2 - Лабораторная установка в собранном виде
3. Зарисовать форму кристаллов для исследованных солей (сделать фотографии).
4. Отчёт о проделанной работе оформить в виде таблицы (Таблица 1), для работы можно использовать объективы с кратным увеличением ×10, ×50, ×100 или ×200, в качестве отправной точки советуем использовать увеличение ×50, которое является стандартным для используемой модели микроскопа.
Таблица 1 - Пример оформления таблицы по микроскопии
Соль | Форма кристаллов | Цвет, прозрачность, морфология | Фото |
NaCl | Ученики должны выполнить задание самостоятельно, используя знания, полученные на уроках геометрии. | рис. 3 | |
CuSO4 ×5H2O | рис. 4 | ||
Na2CO3 | рис. 5 | ||

Рисунок 3 - Кристаллы NaCl

Рисунок 4 - Кристаллы CuSO4×5H2O
В данной работе можно использовать не только уже готовые кристаллы солей, но и вырастить их из растворов, тогда процесс будет более увлекательным для ученика.
2. Приготовление растворов солей
Приготовление растворов солей включает в себя точный расчет количества растворяемого вещества в зависимости от необходимой концентрации, после чего взвешивают нужное количество соли и постепенно растворяют его в воде при постоянном помешивании, соблюдая температурные условия для обеспечения полной растворимости. Важно использовать мерные приборы для точного измерения объема воды и соблюдать правила техники безопасности. Такой процесс обеспечивает однородность раствора, необходимую для проведения последующих химических опытов и наблюдений.
Цель: научиться пользоваться электронными весами, приготовить 1% раствор исследуемой соли.
Материалы для исследования: кристаллы солей NaCl, CuSO4 ×5H2O, Na2CO3.
Реактивы, посуда, оборудование: электронные весы, лабораторные стаканы (100 мл), лодочка для взвешивания, исследуемые соли.
Ход работы:
1. Включить электронные весы, поместить на них лодочку для взвешивания, сбросить весы на отметку 0.
2. Отобрать навеску соли, необходимую для приготовления 100 мл 1% раствора.
3. Аккуратно перенести взятую навеску в пустой стакан, перенести количественно, добавить воды до метки.
4. Отчёт о проделанной работе оформить в виде таблицы (Таблица 2).
Таблица 2 - Пример оформления таблицы по приготовлению растворов солей
Соль | Процентное содержание вещества (указывается учителем) | Масса навески, г. (округлите до целого) |
NaCl | 1% | ≈1 грамм |
CuSO4×5H2O | 1% | ≈1 грамм |
Na2CO3 | 1% | ≈1 грамм |
5. Сделать краткий вывод по проделанной работе.
3. Измерение кислотности среды с помощью pH-метра
Водородный показатель — величина, определяющая концентрацию ионов водорода в растворах, численно равна отрицательному десятичному логарифму молярной концентрации ионов водорода рН = -1g[H+]. pH-метр погружают в исследуемый раствор, на дисплее фиксируют значение pH – числовое выражение уровня кислотности или щелочности среды, где pH < 7 указывает на кислотную, = 7 – нейтральную, а > 7 — щелочную среду. Такой метод позволяет быстро и точно определить свойства раствора, что важно для проведения химических анализов.
Цель: измерить pH раствора соли.
Материалы для исследования: растворы солей NaCl, CuSO4, CaCO3.
Реактивы, посуда, оборудование: лабораторные стаканы (100 мл), pH-датчик (pH-BTA, Vernier, США, на рис. 12), устройство измерения и обработки экспериментальных данных (Vernier LABQ LabQuest, США, на рис. 13).

Рисунок 12 - pH-метр (pH-BTA, Vernier, США)
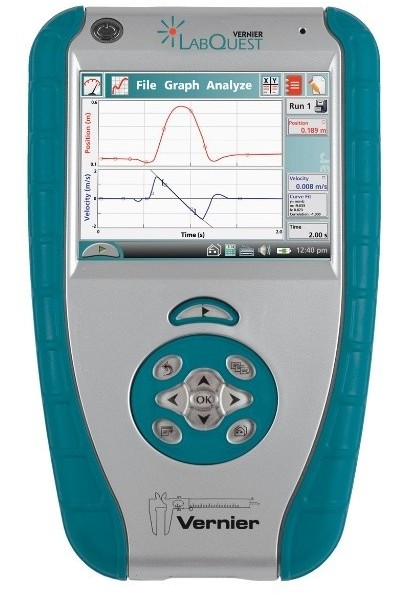
Рисунок 13 - Устройство измерения и обработки экспериментальных данных (Vernier LABQ LabQuest, США)
1. Собрать лабораторную установку, подсоединив pH-метр к устройству измерения и обработки экспериментальных данных, дождаться отображения датчика на дисплее.
2. Погрузить датчик в дистиллированную воду, подождать 1-2 минуты для корректного проведения измерений, записать необходимые экспериментальные значения.
3. Погрузить датчик в экспериментальный раствор, подождать 1-2 минуты, записать необходимые экспериментальные значения, после использования ополоснуть дистиллированной водой;
4. Отчёт о проделанной работе оформить в виде таблицы (Таблица 3), помимо значения pH также привести уравнение диссоциации и гидролиза;
Таблица 3 - Пример оформления таблицы по кислотности
Вещество | pH {данные для примера} | Диссоциация (напишите уравнение) | Гидролиз (напишите уравнение) |
Вода | ≈7,2 | – | – |
NaCl | ≈7,1 | NaCl → Na+ + Cl- | Не гидролизуется |
CuSO4 | ≈5,1 | CuSO4 → Cu2+ + SO42- | Гидролиз по катиону, среда слабокислая, Cu2+ + H2O ⇄ CuOH+ + H+ |
Na2CO3 | ≈9,2 | Na2CO3 → 2Na+ + CO32- | Гидролиз по аниону, среда слабощелочная, CO32- + H2O ⇄ HCO3- + OH- |
5. Сделать краткий вывод по проделанной работе.
6. Ответить на вопрос «Чем обусловлено изменение кислотности раствора по сравнению с водой?».
4. Измерение электропроводности среды с помощью кондуктометра
Электропроводность — это способность водного раствора проводить электрический ток, этот параметр соответственно пропорционален концентрации растворенных минеральных солей. Кондуктометр состоит из двух электродов, погруженных в исследуемый раствор, и прибора, измеряющего сопротивление или проводимость. Перед началом измерений прибор необходимо калибровать на стандартных растворах с известной электропроводностью. После этого электрод аккуратно погружают в раствор, избегая пузырьков воздуха и механических повреждений, и фиксируют показания прибора. Полученные данные позволяют оценить концентрацию растворенных веществ и контролировать качество растворов по стандартным значениям (например, жесткость воды) в химических, биологических и промышленных процессах.
Цель: измерить электропроводность раствора соли.
Материалы для исследования: растворы солей NaCl, CuSO4 ×5H2O, Na2CO3.
Реактивы, посуда, оборудование: лабораторные стаканы (100 мл), датчик электропроводности-кондуктометр (CON-BTA, Vernier, США на рис. 14), устройство измерения и обработки экспериментальных данных (Vernier LABQ LabQuest, США на рис. 13), исследуемые соли.

Рисунок 14 - Датчик электропроводности-кондуктометр (CON-BTA, Vernier, США)
1. Собрать лабораторную установку, подсоединив кондуктометр к устройству измерения и обработки экспериментальных данных, дождаться отображения датчика на дисплее.
2. Погрузить датчик в дистиллированную воду, подождать 1–2 минуты для корректного проведения измерений, записать необходимые экспериментальные значения.
3. Погрузить датчик в экспериментальный раствор, подождать 1–2 минуты, записать необходимые экспериментальные значения, после использования ополоснуть дистиллированной водой.
4. Отчёт о проделанной работе оформить в виде таблицы (Таблица 4), помимо значения электропроводности также привести уравнение диссоциации.
Таблица 4 - Пример оформления таблицы по электропроводности
Вещество | Диссоциация (напишите уравнение) | Электропроводность, мкСм/см {данные для примера} |
Вода | – | ≈262 |
NaCl | NaCl → Na+ + Cl- | ≈277 |
CuSO4 | CuSO4 → Cu2+ + SO42- | ≈281 |
Na2CO3 | Na2CO3 → 2Na+ + CO32- | ≈282 |
5. Сделать краткий вывод по проделанной работе.
6. Ответить на вопрос «Чем обусловлен рост электропроводности раствора по сравнению с водой?».
5. Термометрия с использованием термопары
Термометрия растворов солей включает измерение их температуры с целью контроля тепловых свойств, таких как растворимость и кристаллизация. Для этого используют стандартные термометры или электронные приборы, что помогает определить, например, точку плавления, стабильность раствора, изменение его характеристик от температуры и обеспечить правильные условия хранения и использования в химической и технологической сферах.
Цель: измерить температуру раствора соли.
Материалы для исследования: растворы солей NaCl, CuSO4 ×5H2O, Na2CO3.
Реактивы, посуда, оборудование: лабораторные стаканы (100 мл), термопара (TCA-BTA, Vernier, США на рис. 15), устройство измерения и обработки экспериментальных данных (Vernier LABQ LabQuest, США на рис. 13), исследуемые соли.

Рисунок 15 - Термопара (TCA-BTA, Vernier, США)
1. Собрать лабораторную установку, подсоединив термопару к устройству измерения и обработки экспериментальных данных, дождаться отображения датчика на дисплее.
2. Погрузить датчик в дистиллированную воду, подождать 1–2 минуты для корректного проведения измерений, записать необходимые экспериментальные значения.
3. Погрузить датчик в экспериментальный раствор, подождать 1–2 минуты, записать необходимые экспериментальные значения, после использования ополоснуть дистиллированной водой.
4. Отчёт о проделанной работе оформить в виде таблицы (Таблица 5).
Таблица 5 - Пример оформления таблицы по термометрии
Вещество | Температура, °С {данные для примера} |
Вода | ≈25,5 |
NaCl | ≈25,5 |
CuSO4 | ≈25,4 |
Na2CO3 | ≈25,3 |
5. Сделать краткий вывод по проделанной работе.
Лабораторная работа по термометрии легко может быть модифицирована:
1) можно не просто измерять температуру готового раствора, а исследовать тепловой эффект, выделяющийся или поглощающийся при растворении соли в воде;
2) перспективным является комплексный анализ поведения соли в воде — изменение pH, электропроводности раствора при изменении температуры, усиление, ослабление гидролиза и прочие эффекты.
6. Подведение общих итогов лабораторной работы, обобщение предыдущих выводов
4. Перспективы дальнейшего развития лабораторных занятий
Перспективы будущего развития лабораторных занятий по химии в средней школе напрямую связаны с развитием современных технологий и подходов к обучению. В эпоху цифровизации особенно важным становится использование виртуальных лабораторий и интерактивных симуляторов, которые позволяют школьникам безопасно экспериментировать, моделировать реакции и наблюдать за процессами, недоступными или опасными в обычных условиях
, . Такой формат в последние годы активно развивается и помогает не только закреплять теоретические знания, но и развивать исследовательский азарт, умение анализировать и делать выводы.Возможно также и скорое внедрение дополненной и виртуальной реальности
, которое даёт возможность ученикам «погрузиться» в молекулярный мир, наблюдать за структурой веществ или сами реакции в трехмерном пространстве в мельчайших деталях. Это безусловно делает обучение более живым, понятным и запоминающимся.Кроме того, активное развитие проектных и проблемных методов обучения, когда школьники сами разрабатывают эксперименты, анализируют результаты и ищут решения, также способствует формированию навыков научного мышления, самостоятельности и креативности
, . В связи с этим в будущем лабораторные работы определённо должны перестать быть выполнением набора стандартных задач — они должны в себе заключать выполнение комплексной задачи с использованием разнообразного оборудования и разных областей школьного кругозора, только тогда качественное выполнение лабораторной работы будет способствовать реализации собственных идей, открытия нестандартных решений исследовательской задачи и формирования исследовательской культуры.В целом, перспективы развития лабораторных занятий в современной школе неотъемлемо связаны с созданием гибкой, интерактивной, многообразной, а также индивидуальной системы обучения, которая может не только повысить интерес к химии, но и сформировать у школьников навыки, необходимые для жизни и профессиональной деятельности в современности.
5. Заключение
В условиях современных педагогических подходов к организации уроков химии лабораторные занятия приобретают всё большее значение как эффективный инструмент формирования практических навыков, исследовательского мышления и научной культуры у школьников. Именно поэтому необходимо качественно пересмотреть подходы к их организации, активно внедряя современные технологии, проектные и исследовательские подходы:
1. Использование цифровых устройств, виртуальных лабораторий и современных приборов (например, pH-метров, кондуктометров, цифровых микроскопов) повышает мотивацию к обучению, облегчает усвоение материала и способствует развитию исследовательских умений и самостоятельности учащихся.
2. Интеграция традиционных методов проведения лабораторных работ с современными приборами и технологиями позволяет сделать такие работы более интересными и доступными для школьников. В разработанных рекомендациях особое внимание уделено использованию цифровых технологий и проектных методик, что способствует формированию гибкой системы практических занятий. Такой подход стимулирует развитие критического мышления, самостоятельности и исследовательских компетенций, а также повышает интерес к изучению химии.
3. В рамках методических рекомендаций представлены образцы лабораторных работ с использованием различного оборудования (цифровой микроскоп, pH-метр, кондуктометр, термопара), что позволяет создавать разнообразные и индивидуализированные работы, соответствующие различным уровням подготовки и интересам учеников.
4. Перспективы и пути развития лабораторных занятий связаны с созданием гибкой, многообразной и индивидуализированной системы обучения, способной подготовить учащихся к жизни и профессиональной деятельности. Различные формы проведения лабораторных работ, изменение условий протекания химических реакций и использование в работе разнообразных веществ позволяет разрабатывать индивидуальные задания и полноценные практикумы, учитывающие интересы и уровень каждого ученика.
Таким образом, внедрение дифференцированного и проектного обучения в рамках обучения химии, а также использование современных технологий и педагогических методов организации лабораторных работ способствует развитию у школьников исследовательских и практических навыков, необходимых для успешной самореализации в современном обществе.
